CaO-Al2O3-MgO-SiO2-Ce2O3,渣系活度计算模型
时间:2023-01-16 12:40:14 来源:天一资源网 本文已影响 人 
俞 成 ,邱吉雨 *,刘承军
(1.多金属共生矿生态化冶金教育部重点实验室,辽宁 沈阳 110819;
2.东北大学冶金学院,辽宁 沈阳 110819)
目前,稀土在钢中的应用处于高速发展阶段,国内外进行了大量的基础研究和工艺研发工作,取得了较为丰硕的成果。研究表明,向钢中添加稀土元素可以显著改善钢材的耐热性、抗腐蚀性及力学性能[1-3]。尽管稀土钢的研究开发已取得显著进展,但不可否认的是,稀土钢的产业化应用至今仍面临严峻挑战。稀土对钢材性能的提升作用主要依赖于稀土在钢中的含量。然而,稀土金属在高温条件下具有强活泼性,极易与炉渣中的SiO2、Na2O 等组元发生反应,造成溶解态稀土含量波动,影响稀土的微合金化效果[4]。
精炼渣的主要组元为CaO-Al2O3-MgO-SiO2,其与含稀土钢液(以Ce 代表稀土元素)反应后形成的渣系主要为CaO-Al2O3-MgO-SiO2-Ce2O3。在对上述渣金反应的研究中,含稀土钢液的热力学数据较为完善,相关瓦格纳活度相互作用系数均得以测量[5-6]。然而,由于含稀土渣系的热力学性质稀缺,该体系组元的活度数据难以有所参考,极大地限制了相关研究工作的开展。
渣系组元活度的研究可分为试验测定和模型计算两种。由于采用试验测定研究渣系的组元活度是一项工作量艰巨的任务,学者们提出许多渣系组元活度的模型计算方法,如:完全离子溶液模型[7]、正规溶液模型[8]和共存理论模型[9]等。其中,共存理论模型[9]自提出以来,在不同渣系的组元活度研究方面得到了广泛应用,取得了与实际较为相符的计算结果[10-11]。该方法通过建立离子、简单分子和复杂分子之间的化学平衡关系,根据已有的化学平衡热力学数据,计算出各组元的质量作用浓度,相当于传统应用的活度。
笔者基于分子离子共存理论,建立了CaOAl2O3-MgO-SiO2-Ce2O3渣系活度计算模型,并绘制了各组元的等活度线图,讨论了各熔渣组元对于钢中溶解态稀土含量波动的影响,根据计算结果分析了低反应性熔渣的设计方向,研究结果对于稀土钢冶炼具有指导意义。
分子-离子共存理论模型的假设前提和计算步骤可参见张鉴的专著[9],该理论模型应用于CaOAl2O3-MgO-SiO2-Ce2O3渣系时,具体假设前提如下:
1) 熔渣由简单离子(Ca2+、Mg2+、O2-等)和SiO2、硅酸盐、铝酸盐等分子组成;
2) 简单离子和分子间进行了动态平衡反应:(Me2++O2-)+(SiO2)=(MeSiO3);
3) 熔渣内部的化学反应服从质量作用定律。
1.1 熔渣结构单元的确定
建立活度模型首先需要收集渣系内部所有结构单元以及对应的吉布斯自由能数据,以便后续建立化学平衡常数方程。针对CaO-Al2O3-MgO-SiO2-Ce2O3渣系,通过查阅相关文献和相图信息[6,12-13],确定了渣系的结构单元如表1 所示。

表1 CaO-Al2O3-MgO-SiO2-Ce2O3 结构单元Table 1 Structural units of CaO-Al2O3-MgO-SiO2-Ce2O3
表1 中绝大多数化合物热力学数据可通过查阅Factsage 8.1 软件[14]确定。其中,化合物CaO·3SiO2·2Ce2O3的热力学数据缺失,笔者将首先对其进行计算。
1.2 化合物吉布斯自由能的计算
化合物CaO·3SiO2·2Ce2O3的吉布斯自由能可由H298、S298和Cp(T)确定,详见式(1)。
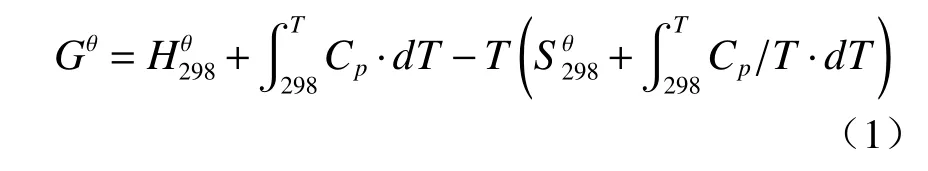
其中,H298、S298可采用Li 等[15]提出的基于笼效应的分裂-组合法计算,采用该方法评估的60 种复杂化合物的G298f、H298f 与热力学手册数值的平均误差分别为0.33%、0.39%,表明该方法预测化合物在298 K 时的G和H具有相当的可信度。Cp(T=298 K)可采用奈曼-柯普定律计算,该定律由Leitner[16]提出,其发现298 K 时300 余种化合物与相关反应物的△Cp(298 K)均在20 J/(mol·K)内,平均值接近于0,故可用相关反应物的Cp(298 K)替代未知多元化合物的Cp(298 K);
在此基础上,Cp(T>298 K)则进一步采用Kubaschewski[17]提出的方法,笔者及所在课题组前期已将该方法应用于2CaO·Al2O3·Ce2O3和2CaO·3Al2O3·Ce2O3的热力学数据计算[18],并得到了与实际数据较为吻合的计算结果。
通过上述方法,计算了CaO·3SiO2·2Ce2O3化合物的热力学数据,并将其应用于活度模型中,计算结果如表2 所示。

表2 CaO·3SiO2·2Ce2O3 化合物的热力学数据Table 2 Thermodynamic data of CaO·3SiO2·2Ce2O3 compounds
1.3 活度计算模型建立
获取了熔渣的结构单元及吉布斯自由能数据后,开始建立化学反应平衡常数方程,以便后续熔渣活度的计算。

由质量平衡定律可知:

由反应前后CaO、Al2O3、MgO、SiO2、Ce2O3的总摩尔数不变可知:
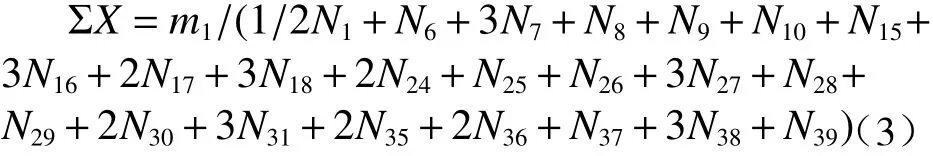
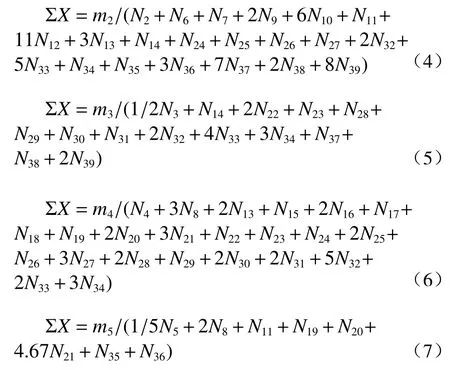
式(2)~(7)即为CaO-Al2O3-MgO-SiO2-Ce2O3渣系的活度计算模型。分子离子共存理论定义作用浓度为传统意义的活度。N6~N39可由N1、N2、N3、N4、N5及对应的反应平衡常数Ki表示(以式(8)、式(9)为例),Ki可通过前文化合物吉布斯自由能数据获取(Ki=exp(-ΔGθ/RT)。最后,通过Matlab 软件中的fslove 函数即可计算所有结构单元的作用浓度。
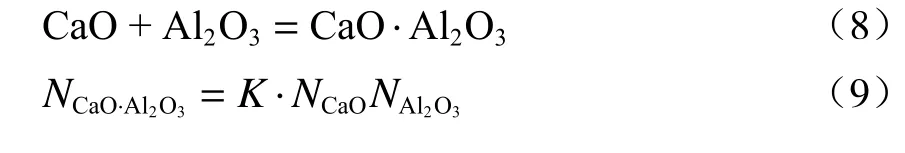
图1 为Factsage 8.1 软件计算所得稀土Ce 与渣中组元CaO、Al2O3、SiO2反应的标准吉布斯自由能曲线,由图1 可知,[Ce]与(SiO2)反应的标准吉布斯自由能要远低于(CaO)和(Al2O3)的相关反应。因此,渣中SiO2活度对于稀土钢的低反应性精炼渣设计至关重要,这与文献[4]提及的含稀土钢液易与熔渣中SiO2反应也较为符合。精炼渣可分为CaO-SiO2基与CaO-Al2O3基两种类型,首先计算了两类渣系的SiO2活度分布,以便确定稀土钢精炼渣的基体选取,便于后续进一步讨论其他组元活度变化。
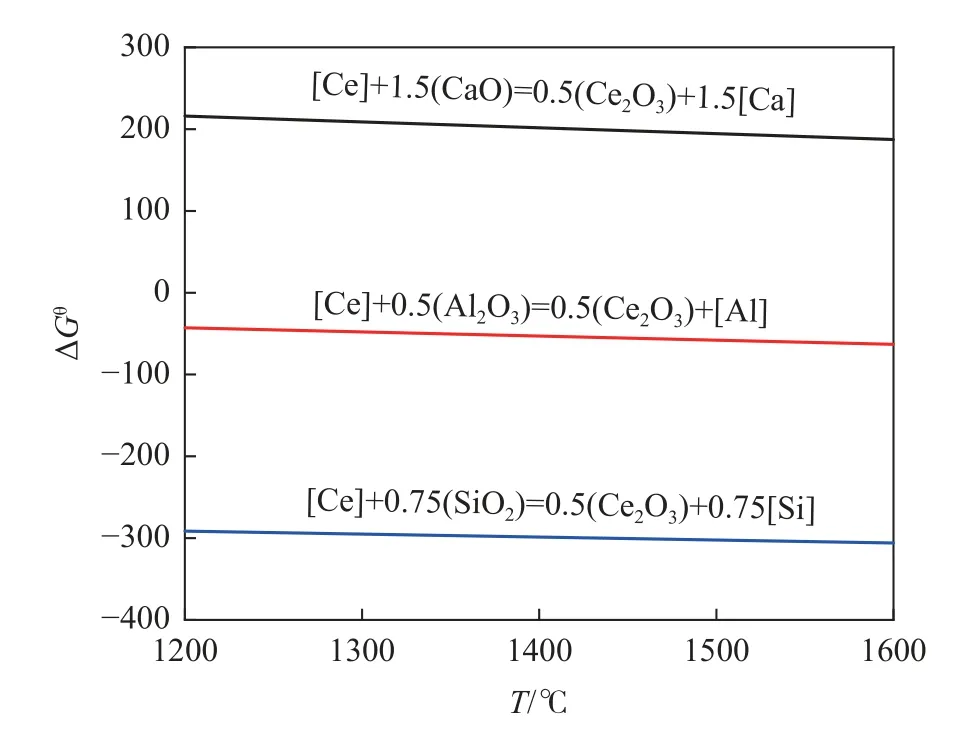
图1 Ce 与CaO、Al2O3、SiO2 反应的标准吉布斯自由能Fig.1 Standard Gibbs free energy of Ce reaction with CaO,Al2O3 and SiO2
2.1 CaO-SiO2 基和CaO-Al2O3 基渣系中的SiO2 活度
为减轻镁质耐材侵蚀,精炼渣中的MgO 质量分数约为5%[19]。本节计算中,对CaO-Al2O3-5%MgO-SiO2-Ce2O3伪四元相图中的CaO-SiO2基成分区域(w(Al2O3)=7%)和CaO-Al2O3基成分区域(w(SiO2)=7%)在精炼温度条件1 600 ℃时,组元SiO2的活度分别进行了计算,相关成分区域如图2所示,计算结果如图3 所示。
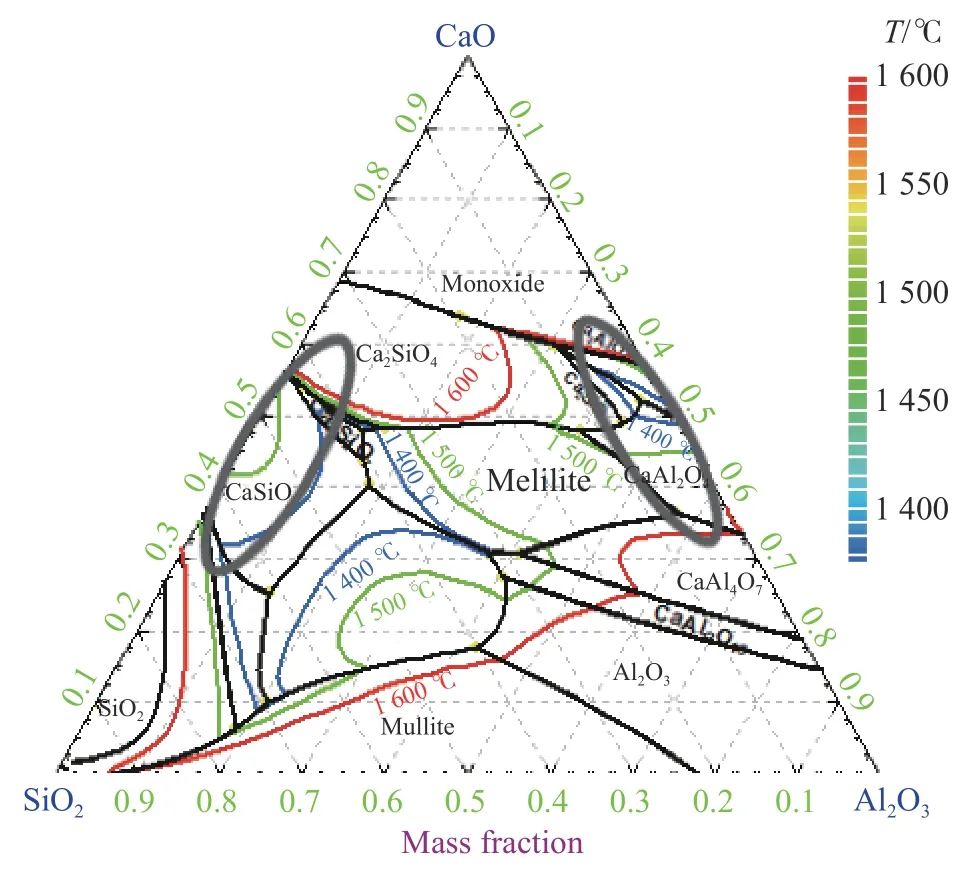
图2 CaO-Al2O3-SiO2 三元相图Fig.2 CaO-Al2O3-SiO2 ternary phase diagram
由图3(a)可知,CaO-Al2O3基精炼渣中的SiO2活度变化范围为4×10-19~ 7×10-18。当w(CaO)/w(Al2O3)一定时,SiO2的活度随w(Ce2O3)升高而增大。当w(Ce2O3)一定时,随着w(CaO)/w(Al2O3)的升高,SiO2活度呈现先减小后增大的趋势,活度最小值所对应的w(CaO)/w(Al2O3)大约为1。由图3(b)可知,CaO-SiO2基精炼渣中的SiO2活度变化范围约为0.003~0.4。当w(CaO)/w(SiO2)一定时,随着w(Ce2O3)的升高,w(SiO2)逐渐降低造成SiO2活度减小。与CaO-Al2O3基相反。当w(Ce2O3)一定时,随着w(CaO)/w(SiO2)的升高,渣中w(SiO2)降低导致SiO2活度逐渐减小。
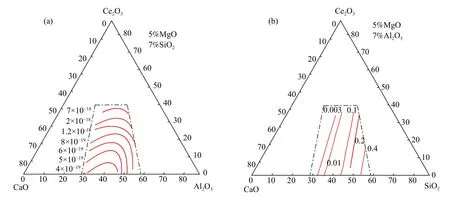
图3 CaO-Al2O3-5%MgO-SiO2-Ce2O3 渣系中SiO2 等活度图Fig.3 Iso-activity diagram of SiO2 in CaO-Al2O3-5%MgO-SiO2-Ce2O3 slag system
根据计算结果可知,CaO-Al2O3基精炼渣的SiO2活度远远小于CaO-SiO2基精炼渣。因此,稀土钢精炼渣采用CaO-Al2O3基渣系可有效抑制Ce与SiO2间的反应。
2.2 CaO-Al2O3-5%MgO-7%SiO2-Ce2O3 渣系组元活度变化规律
由图1 可知,Ce 与Al2O3之间也有一定的反应能力,讨论CaO-Al2O3基渣系中Al2O3活度及反应产物Ce2O3活度对于稀土钢精炼渣设计同样重要。本节将重点讨论w(CaO)/w(Al2O3)和w(Ce2O3)对CaO-Al2O3-5%MgO-7%SiO2-Ce2O3精炼渣中Ce2O3及Al2O3活度的影响。
图4 为1 600 ℃时CaO-Al2O3基精炼渣的Ce2O3等活度图。由图4 可知,当w(CaO)/w(Al2O3)一定时,Ce2O3活度随w(Ce2O3)升高而增大。当w(Ce2O3)一定时,随着w(CaO)/w(Al2O3)的升高,Ce2O3活度逐渐增大。图5 为1 600 ℃时CaOAl2O3基精炼渣的Al2O3等活度图。由图5 可知,当w(CaO)/w(Al2O3)一定时,Al2O3活度随w(Ce2O3)升高而减小。当w(Ce2O3)一定时,随着w(CaO)/w(Al2O3)的升高。渣中w(Al2O3)降低导致Al2O3活度逐渐减小。通过模型计算的Ce2O3及Al2O3活度变化规律与Kitano[6]等的试验结果保持一致,Kitano 提到该变化规律是由于CaO-Al2O3-Ce2O3熔渣内Al2O3呈酸性,CaO、Ce2O3呈碱性造成的。
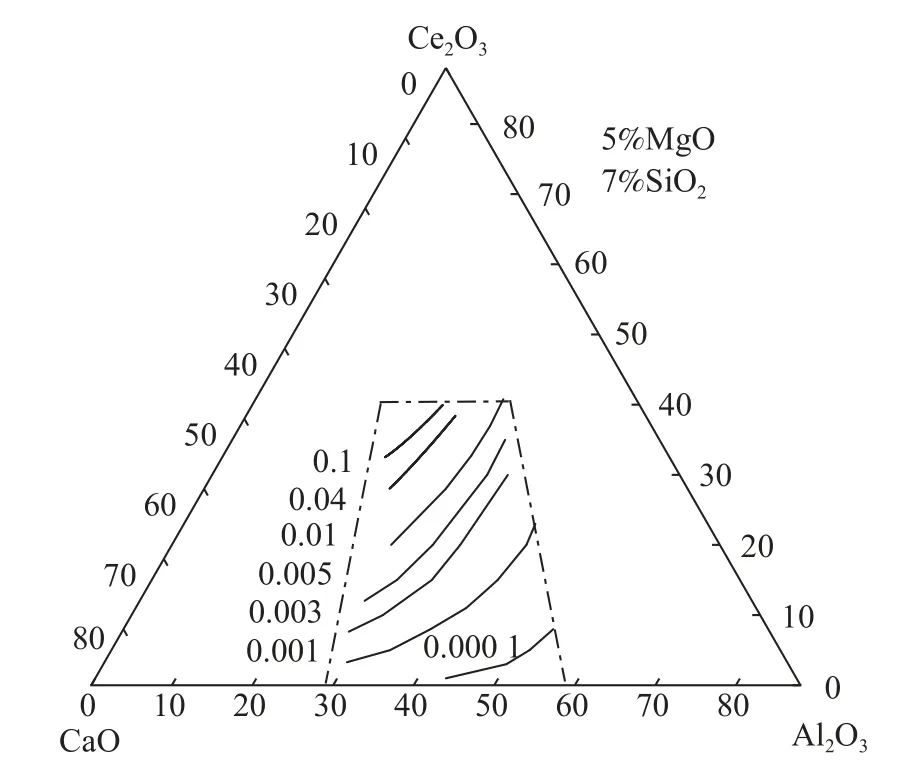
图4 CaO-Al2O3-5%MgO-7%SiO2-Ce2O3 渣系中Ce2O3 等活度图Fig.4 Iso-activity diagram of Ce2O3 in CaO-Al2O3-5%MgO-7%SiO2-Ce2O3 slag system
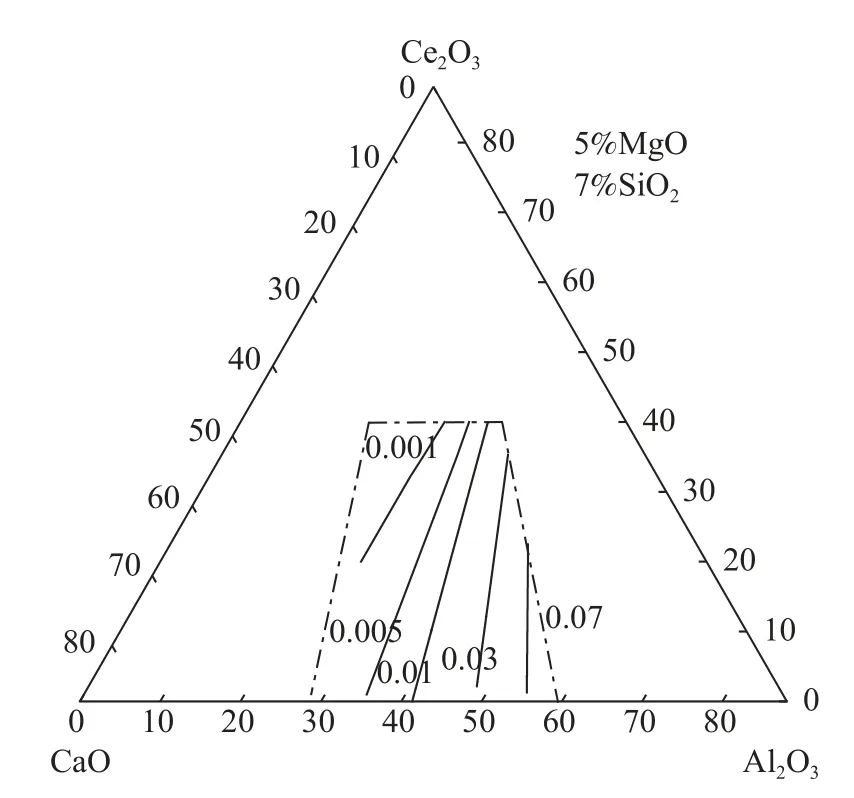
图5 CaO-Al2O3-5%MgO-7%SiO2-Ce2O3 渣系Al2O3 等 活度图Fig.5 Iso-activity diagram of Al2O3 in CaO-Al2O3-5%MgO-7%SiO2-Ce2O3 slag system
根据上述计算结果可知,渣中w(CaO)/w(Al2O3)和w(Ce2O3)升高可增大Ce2O3活度、减小Al2O3活度。根据Ce 与Al2O3间的反应表达式(10)可知,提高Ce2O3活度、降低Al2O3活度可有效抑制反应向右进行。因此,提高渣中w(CaO)/w(Al2O3)和w(Ce2O3)可有效降低稀土钢与精炼渣间的渣金反应。
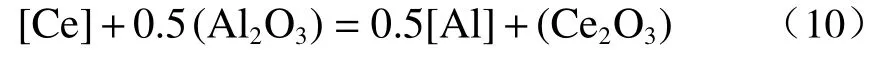
采用分裂-组合法、奈曼-柯普定律及Kubaschewski 法计算了化合物CaO·3SiO2·2Ce2O3的H298、S298和Cp(T);
基于分子离子共存理论建立了CaOAl2O3-MgO-SiO2-Ce2O3活度计算模型,得到如下结论:
1) CaO·3SiO2·2Ce2O3的H298和S298分别为-7 300.568 kJ/mol、466.137 J/(mol·K),Cp(T)=477.948+67.814×10-3T-88.2×105T-2。
2) CaO-Al2O3基精炼渣的SiO2活度范围(4×10-19~ 7×10-18)远小于CaO-SiO2基精炼渣的活度范围(0.003~0.4),为抑制含稀土钢液与熔渣中SiO2的反应,稀土钢精炼渣应采用CaO-Al2O3基渣系。
3) 对于CaO-Al2O3基精炼渣,提高w(CaO)/w(Al2O3)和w(Ce2O3)可增加Ce2O3活度、减小Al2O3活度,能够减弱含稀土钢液与熔渣中Al2O3间的反应。
致谢
本研究开展过程中得到了如下基金的资助,在此表示感谢:国家自然科学基金联合基金项目(U1908224)、博士后基金面上基金项目(N2125019)、中央高校基本科研业务费项目科研启动与科研水平提升项目(ZX20210021)、辽宁省“兴辽英才计划”项目(XLYC2002047)。
猜你喜欢 热力学稀土化合物 航空航天类“工程热力学”课程思政建设的探索与实践大学·课外阅读(2022年3期)2022-04-25王牌稀 土科学大观园(2019年13期)2019-09-10例析高考中的铁及其化合物中学化学(2017年6期)2017-10-16例谈氯及其化合物的学习与考查中学化学(2017年6期)2017-10-16钒及其化合物在高考中的考查中学化学(2017年2期)2017-04-01对真实气体热力学过程的探究中国科技纵横(2017年3期)2017-03-29金属元素及其化合物试题与研究·高考理综化学(2016年3期)2017-03-28实测冰水侧向界面热力学融化速率南水北调与水利科技(2016年6期)2017-01-062020年我国稀土年度开采量将控制在14万吨以内中国经济周刊(2016年41期)2016-10-28促进物理思维训练的好题中学生数理化·高二版(2008年10期)2008-06-17 相关关键词: 纯Python实现鸢尾属植物数据集神经网络模型 初中数学几何模型 极限单车运动su模型 数学模型举例 角平分线四大模型









